Ambas oferecem uma reposição eficiente de ferro para tratar anemia ferropriva em diversas condições clínicas, incluindo insuficiência renal crônica, perdas sanguíneas e intolerância ao ferro oral.
Mecanismo de ação
É um complexo de ferro utilizado para reposição intravenosa em casos de anemia ferropriva. Projetada para liberar ferro de forma controlada e minimizar a toxicidade, formando uma matriz que regula a liberação do ferro. Após a administração intravenosa, o ferro é distribuído para o sistema reticuloendotelial, liberado gradualmente e excretado principalmente pelas fezes. Sua farmacocinética permite a administração de altas doses em uma única infusão, com meia-vida terminal de 7 a 12 horas e tempo de residência de 11 a 17 horas. É eficaz em pacientes com anemia associada a condições crônicas ou má absorção de ferro via oral, como insuficiência renal, doenças inflamatórias, e após cirurgia bariátrica, otimizando a reposição de ferro e reduzindo a necessidade de transfusões.
Indicação
Anemia Ferropriva em Pacientes com Insuficiência Renal Crônica: A carboximaltose férrica é indicada para pacientes com insuficiência renal crônica que desenvolvem anemia ferropriva devido à dificuldade do organismo em mobilizar ferro, comum em doenças inflamatórias crônicas como artrite reumatoide e doença inflamatória intestinal.
Anemia Ferropriva em Pacientes com Perdas Sanguíneas Agudas ou Crônicas: Em casos de anemia ferropriva causada por perdas sanguíneas agudas ou crônicas, podem ser utilizadas para uma rápida e eficiente reposição de ferro.
Anemia Ferropriva em Pacientes com Intolerância ou Falha ao Tratamento Oral: Para pacientes que não toleram ou falham no tratamento oral de ferro, oferecem uma alternativa eficaz com
administração intravenosa.
Anemia Ferropriva em Pacientes Pré e Pós-Operatórios: ambas indicam uma correção rápida da anemia ferropriva em pacientes antes e após procedimentos cirúrgicos, ajudando na recuperação e na manutenção dos níveis de ferro.
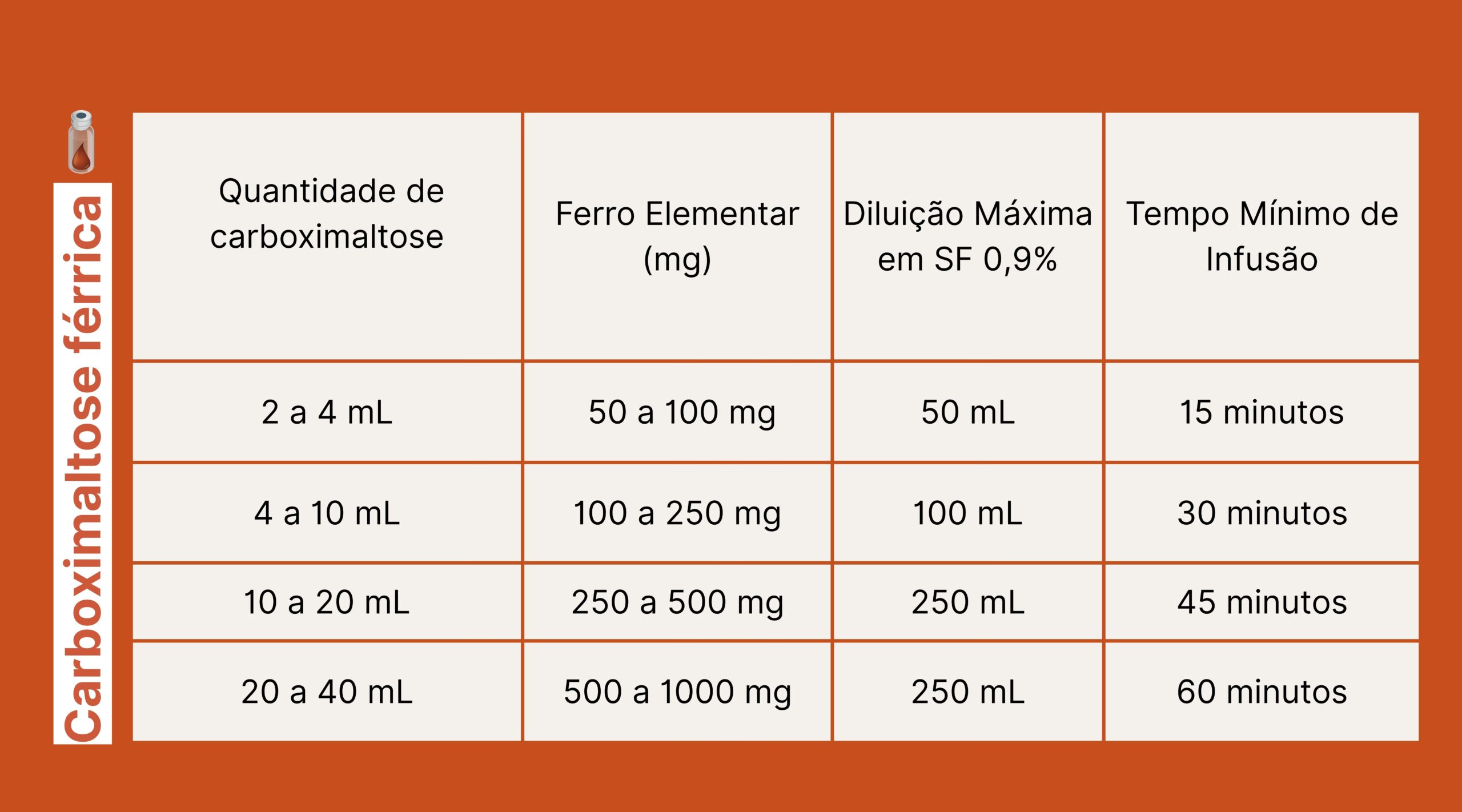
Carboximaltose férrica
A dose de carboximaltose férrica deve ser determinada pelo médico com base no peso corporal e níveis de hemoglobina do paciente. Para pacientes com menos de 35 kg, a dose não deve exceder 500 mg. Em pacientes com hemoglobina ≥ 14 g/dL, recomenda-se uma dose inicial de 500 mg, com monitoramento dos níveis de ferro.
A dose única máxima é de 1.000 mg (40 mL) por dia ou 20 mg/kg de peso corporal, e não deve ser administrada mais de uma vez por semana.
A administração intravenosa pode ser feita por injeção ou infusão. Para injeções, doses até 200 mg não têm tempo específico, entre 200 mg e 500 mg deve ser administrada a 100 mg/min, e doses entre 500 mg e 1.000 mg devem ser dadas em 15 minutos. A infusão pode ser de até 1.000 mg (40 mL). A carboximaltose férrica deve ser diluída apenas em solução estéril de cloreto de sódio 0,9% e infundida lentamente a 30-40 gotas/min. Antes da administração, a solução deve ser inspecionada para garantir que está homogênea e livre de sedimentos. A sugestão de uso geral é de 250 mg (10 mL) diluídos em 100 mL de SF 0,9% e infundidos em 30 minutos.
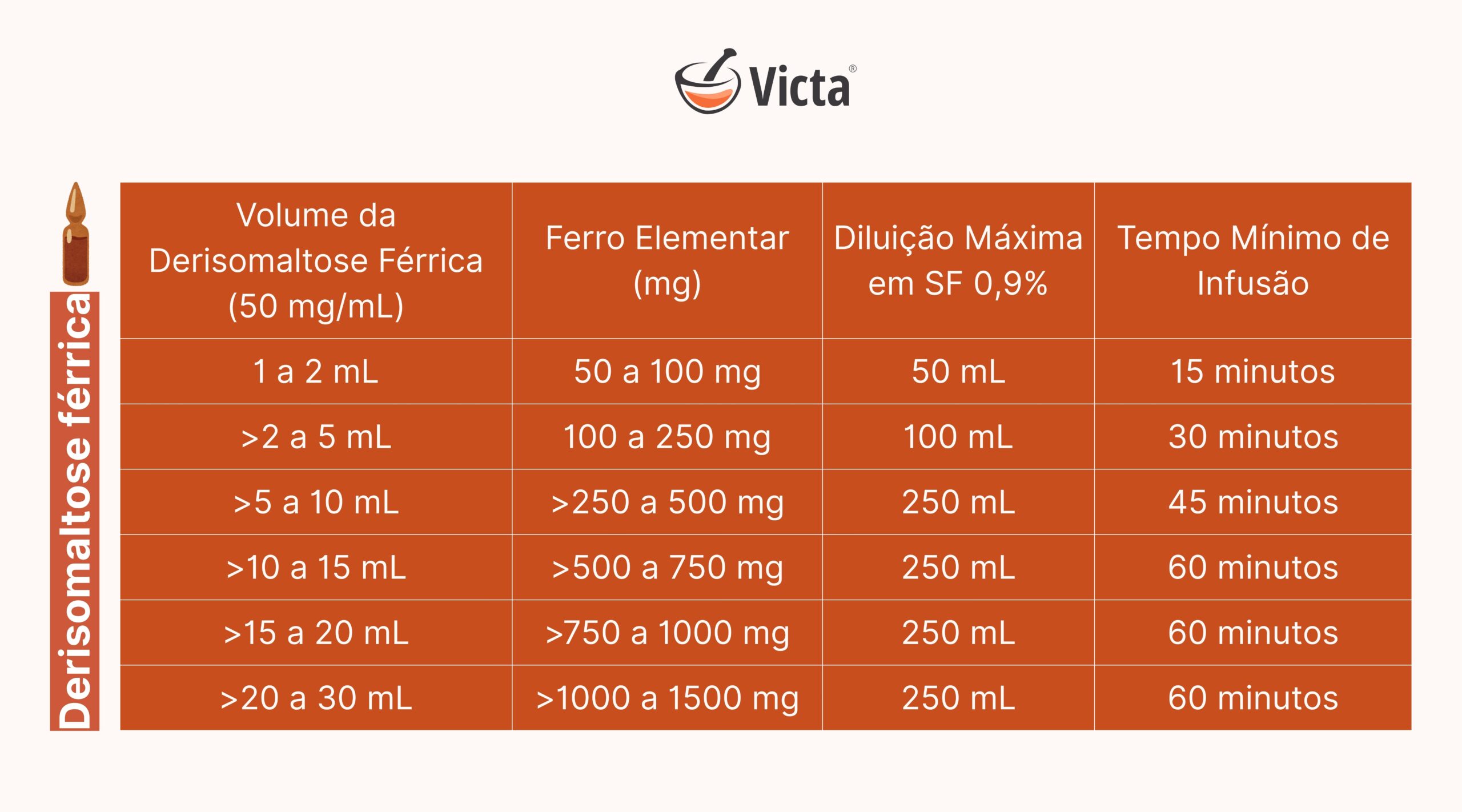
Derisomaltose férrica
A derisomaltose férrica é uma formulação intravenosa moderna e altamente estável, indicada para reposição de ferro em pacientes com deficiência documentada. Por permitir doses elevadas em uma única infusão, seu uso favorece maior adesão e eficácia clínica. Entretanto, é essencial observar os limites de segurança relacionados à dose total e ao peso corporal do paciente.
Recomendações de dosagem. A dose recomendada é de até 20 mg de ferro elementar/kg de peso corporal, podendo ser administrada em infusão única.
Não ultrapassar 1500 mg por infusão.
Caso a dose total calculada ultrapasse 20 mg/kg ou 1500 mg, recomenda-se fracionar a administração em duas infusões, com um intervalo de pelo menos 7 dias
entre as aplicações.Exemplo clínico: Paciente com 85 kg → 85 × 20 mg = 1700 mg de ferro necessário
Recomenda-se administrar duas infusões de 850 mg, com intervalo de uma semana.Os estudos pré-clínicos indicam que não apresentam riscos especiais para humanos em termos de farmacologia de segurança, toxicidade ou genotoxicidade. O
ferro atravessa a barreira placentária e é excretado no leite em quantidades controladas.No entanto, a administração intravenosa pode provocar reações de hipersensibilidade. Reações adversas devem ser monitoradas por pelo menos 30 minutos após a
aplicação. É crucial evitar extravasamento venoso para prevenir hiperpigmentação e irritação cutânea.


Sem comentários